일을 하다보면 자주 찾는 사이트가 생기기 마련인데, 신입 병아리 때는 하나하나 기억을 더듬어가면서 찾아 들어가곤 했지만 크롬의 북마크바(크롬 우측상단의 ☆모양을 클릭해서 "현재 탭을 북마크에 추가")를 이용하면 상단바 클릭 한 번에 들어갈 수 있다는 간단한 팁을 알고난 이후부터는 아주 편하게 사이트를 추가해 이용하고 있다. 내가 북마크바에 추가한 사이트를 아래에 공유하며, 이후 업무를 진행하면서 더 추가하는 사이트는 여기에도 업데이트하도록 하겠다.
의약품안전나라 (https://nedrug.mfds.go.kr/)
의약품의 전자민원/전자보고를 신청할 수 있는 민원 신청 사이트이자, 임상시험 정보, 의약품 정보, 품목허가 현황 등을 확인하는 용도로 자주 찾는 사이트이다. 최근에는 의약품 정보에서 대한민국약전의 내용을 편리한 검색 기능으로 찾아볼 수 있어 잘 이용하고 있다. (이전에는 약전 PDF를 다운받아 열기만해도 내용이 방대해서 로딩에 시간이 많이 걸리곤 했는데 이 사이트에서는 원하는 목차에서 바로바로 검색할 수 있어 효율적이다.) 의약품안전나라 사이트는 링크 주소에 따라 보통 "애니드럭(NEdrug)"이라고 부른다.

의료기기 전자민원창구 (https://udiportal.mfds.go.kr/msismext/emd/min/mainView.do)
나는 의약품을 담당하고 있기 때문에 의료기기 민원창구는 이용할 일이 거의 없지만, 위의 의약품 민원창구와 별개로 존재하는 사이트이기에 참고용으로 작성한다. 해당 시스템이 2023-02-27부터 개편되어 의료기기 전자민원창구 접속 시 아래와 같은 화면을 확인할 수 있다.

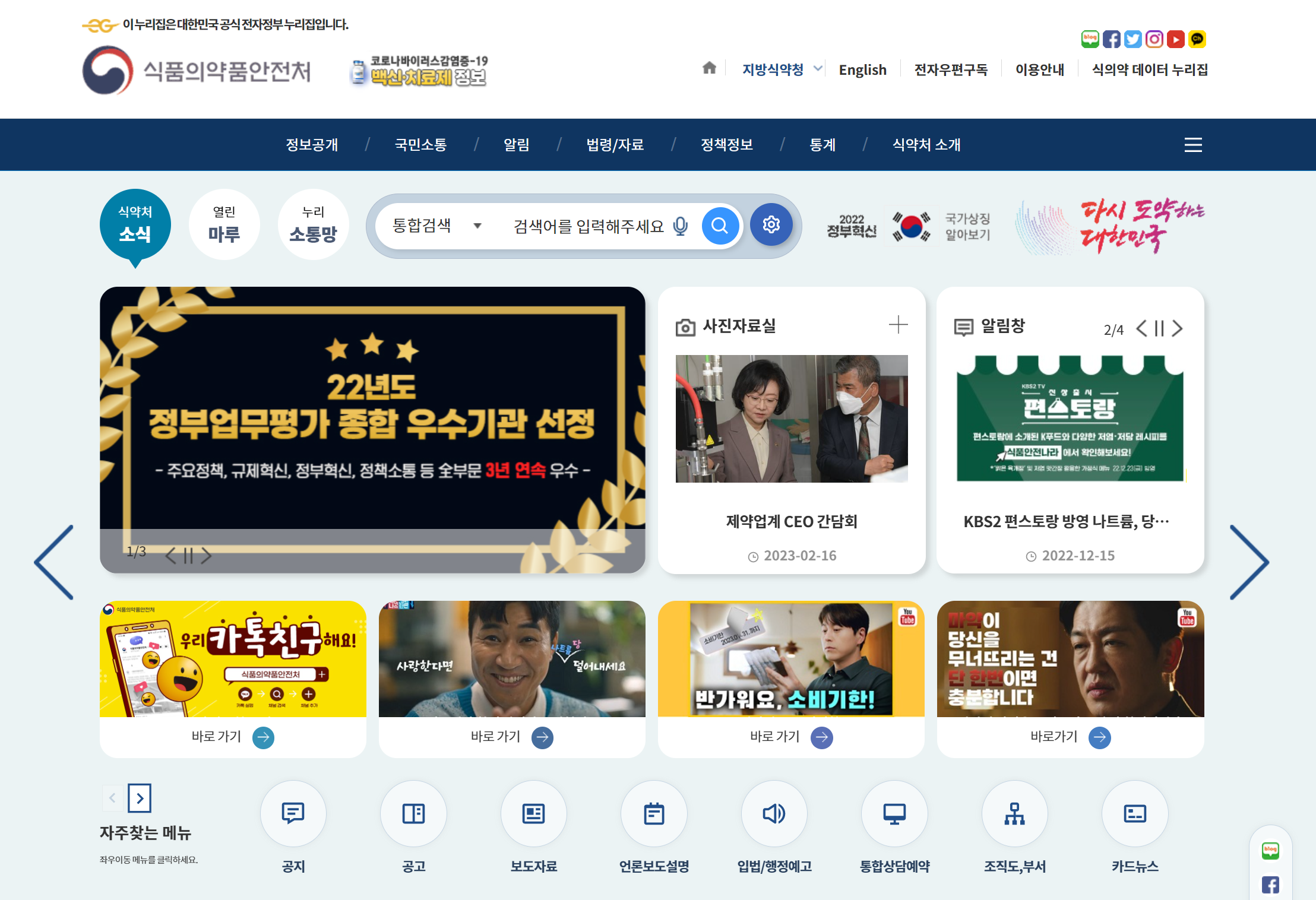
식품의약품안전처 (https://www.mfds.go.kr/)
한국의 식품의약품안전처(Ministry of Food and Drug Safety, MFDS) 홈페이지이다. 여기서는 주로 법령/자료의 공무원지침서, 민원인안내서 등 가이드라인을 찾아보는 편이다. 진행 중인 민원이 있는 경우에는 담당자와 연락을 위해 식약처 소개의 조직도, 부서 탭을 주로 이용하고 있다.
식품의약품안전평가원 직원검색
(https://www.nifds.go.kr/www/377/member/list.do)
작년까지 각 부서별 대표번호 시행으로, 직원별로 담당업무와 전화번호를 확인할 수 있던 이전과는 달리 대표번호로만 연락이 가능하고 그 마저도 집중근무 시행으로 아주 간헐적으로만 연락이 가능했던 시기가 있었으나, 얼마 전 대표번호 시행은 중단되었다. 허나, 식약처 홈페이지에서는 몇몇 평가원 부서 중 대표번호가 남아있어 불편하고 부서별 직원을 검색하기 위해서는 각 부서를 클릭, 대표 연락처 클릭하고 검색 또는 페이지를 넘겨가며 조회를 해야해서 번거로웠는데, 이 직원검색 사이트를 북마크에 추가하여 사용하니 한 번에 평가원 모든 부서의 직원 검색이 가능하여 추천한다.

국가법령정보센터, 법제처 (https://www.law.go.kr/)
우리나라의 모든 법령정보를 제공하는 사이트이니만큼, RA 업무에 필요한 규정의 최신 버전과 법령체계도, 제정개정이유, 별표나 서식 등을 모두 볼 수 있는 사이트이다. 회사에서는 필요에 따라 규정을 다운받아 공용으로 보관하기도 하고, PCB (Pharmaceutical Code Book) 핸드북을 구매하기도 하는데, 그렇게 찾는 것 보다는 법제처 사이트에서 한번에 검색하는 것이 최신의 규정을 확인할 수 있고 빨라서 효율적이다. 단, PCB 핸드북의 경우 어떤 규정을 참고해야할 지 모르는 신입들에게는 줄치고 표시해가면서 익히기 좋다. 초반에는 규정을 모아둔 자료들을 바탕으로 공부하며 각 상황에 따라 참고해야하는 규정이 어느정도 익혀지면 법제처 사이트에서 최신 규정을 확인하는 방식으로 진행하게 된다.

아래부터는 필수사항은 아니지만, 규제동향이나 교육, 행사 정보를 참고할 수 있는 사이트이다.
한국제약바이오협회 (https://www.kpbma.or.kr/)
알림&신청의 공지사항에서 식약처 (실태조사, 생산실적 등) 협조 공문, 제약 관련 교육, 식약처 등 규제기관 주관 행사 정보 등을 얻을 수 있어 많이 사용하고 있다. 공지사항 탭은 회원사인 경우에만 내용 열람이 가능한데, 2023년 02월 기준으로 KPBMA 협회의 회원사 중 정회원은 188곳, 준회원은 80곳(중복 포함)의 제약회사 혹은 CRO 등이 가입되어 있으니, 현직 RA라면 회사 ID로 모니터링을 하고 필요한 자료에 대해 배포하기도 한다. 이 외에도 제약관련 뉴스, 카드뉴스 등 여러 사이트에 들어가서 검색이 필요한 자료들이 정리되어 있어서 참고하기 편하다.
한국바이오의약품협회 (https://www.kobia.kr/)
교육 및 행사를 일정표 형식으로 볼 수 있어 직관적이며, 위의 한국제약바이오협회와 중복되지 않는 교육이나 행사정보가 꽤 올라오고 있기 때문에 KoBIA 홈페이지에서도 참고하는 편이다. 특히 이 협회에서 다이나믹바이오 (Dynamic BIO) 행사를 매년 진행하고 있고 해당 행사에서 ICH 가이드라인교육을 몇 일간 진행한다. 그 자료는 교육 및 행사자료 탭에서 확인할 수 있다. 또한 약사법에 따라 제조수입관리자는 2년 주기로 16시간 이상 교육을 이수해야 하는데, 그 교육을 제조수입관리자교육 탭에서 신청할 수 있다.
'의약품 인허가' 카테고리의 다른 글
| 의약품 임상시험계획승인(IND) [3] 신청서 상세 작성방법 (0) | 2023.02.21 |
|---|---|
| 의약품 임상시험계획승인(IND) [2] 의약품안전나라 로그인 후 민원신청까지 (0) | 2023.02.20 |
| 의약품 임상시험계획승인(IND) [1] 제출자료 범위 (0) | 2023.02.17 |
| 의약품 분류와 민원신청 (with 융복합의료제품 판단) (0) | 2021.12.03 |
| 소소한 RA 팁들 공유예정 (0) | 2021.12.02 |




댓글