약 한달만에 돌아온 2탄. RAPS RAC가 무엇인지 모르겠다면 빠르게 아래 1탄을 보고 와요.
2024.03.01 - [RAC 자격증] - RAPS RAC 자격증 알아보기 (1) 자격요건, 시험정보
RAPS RAC 자격증 알아보기 (1) 자격요건, 시험정보
인허가 업계에서 몇 년동안 종사했다면 들어봤을만한 RAC 자격증. 나의 버킷리스트에 항상 RAC 자격증 취득이 있었는데... 과연 언제 딸 수 있을지... 오늘은 2024 Candidate Guide를 바탕으로 의약품 RAC
workingpeach.tistory.com
보고 왔다면 오늘은 RAC 시험 중 Drug 분야의 공부 체크리스트를 알아보겠다.
RAPS 홈페이지 > Certifications > RAC > Exam Preparation으로 들어가면 준비단계가 나오는데, 그 중 1. Prepare으로 가면 어떻게 RAC 시험을 준비해야 하는지 확인이 가능하다.

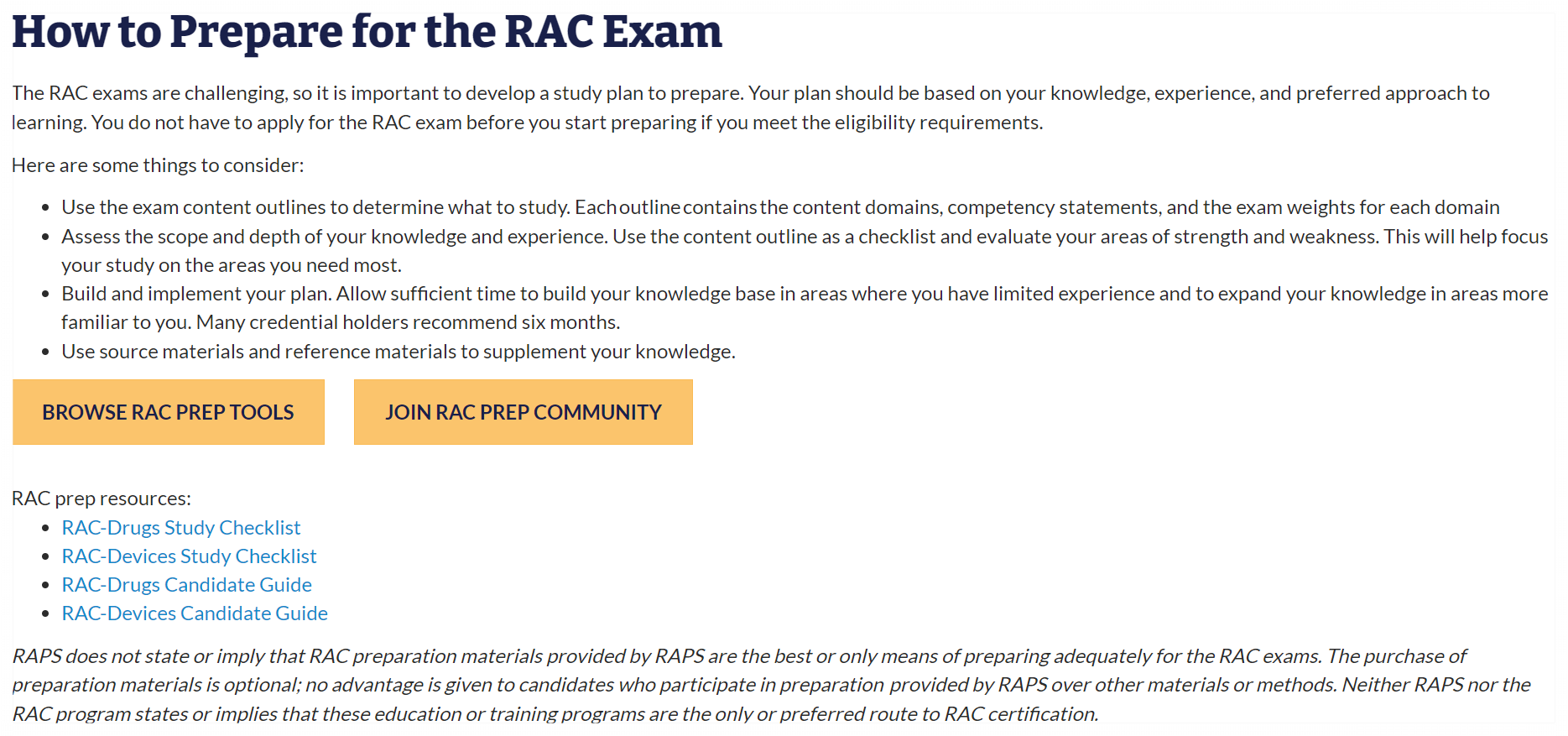
위 설명을 한글로 좀 정리해보았다. 더보기 ▼ 클릭
The RAC exams are challenging, so it is important to develop a study plan to prepare. Your plan should be based on your knowledge, experience, and preferred approach to learning. You do not have to apply for the RAC exam before you start preparing if you meet the eligibility requirements. Here are some things to consider:
RAC 시험은 난이도가 있기 때문에 준비를 위한 공부 계획을 세우는 것이 중요하다. 본인의 지식, 경험 및 선호하는 학습 방식을 기반으로 계획을 세워야 한다. 이 때 고려해야 할 몇 가지 사항이 있다.
- Use the exam content outlines to determine what to study. Each outline contains the content domains, competency statements, and the exam weights for each domain
시험 내용 개요를 사용하여 무엇을 공부할지 결정하여야 한다. 각 개요에는 내용 도메인, 역량 문항 및 각 도메인의 시험 가중치가 포함되어 있다.
- Assess the scope and depth of your knowledge and experience. Use the content outline as a checklist and evaluate your areas of strength and weakness. This will help focus your study on the areas you need most.
기존 본인이 가지고 있는 지식 및 경험의 범위, 깊이를 평가하여야 한다. 체크리스트로 활용하여 강점과 약점을 평가할 수 있다. 이는 가장 필요한 영역에 중점을 두고 공부하는 데 도움이 된다.
- Build and implement your plan. Allow sufficient time to build your knowledge base in areas where you have limited experience and to expand your knowledge in areas more familiar to you. Many credential holders recommend six months.
계획을 세우고 실행하여야 한다. 경험이 적은 분야라면 지식을 습득하고, 익숙한 분야에서는 지식을 확장하는 데 충분한 시간을 들여야 한다. 많은 자격증 소지자들은 이에 6개월을 권장한다.
- Use source materials and reference materials to supplement your knowledge.
지식을 보완하기 위해 소스 자료 및 참고 자료를 활용할 수 있다.
- RAPS does not state or imply that RAC preparation materials provided by RAPS are the best or only means of preparing adequately for the RAC exams. The purchase of preparation materials is optional; no advantage is given to candidates who participate in preparation provided by RAPS over other materials or methods. Neither RAPS nor the RAC program states or implies that these education or training programs are the only or preferred route to RAC certification.
RAPS에서 제공하는 RAC 준비 자료가 RAC 시험을 적절하게 준비하는 최선 또는 유일한 수단은 아니다. 준비자료 구매는 선택 사항이다. RAPS가 제공하는 준비자료는 다른 자료나 방법에 비해 어떠한 이점도 주어지지 않는다.
위에서 언급된 본인 평가용 체크리스트는 위 화면의 RAC prep resources: RAC-Drugs Study Checklist (파란색 링크)를 클릭하면 확인할 수 있다. 4개의 도메인 항목으로 크게 나눠볼 수 있는데, 내용이 많아서 도메인 별로 각각 포스팅 해보겠다.
다음 체크리스트 항목들 각각에 대해 이해하고 내가 얼마나 이해하고 있는 지 3단계로 표시해볼 수 있다.

Domain I: Strategic Planning – Exam Weighting approximately 24%
다음은 시험 문제의 24% 비중을 차지하는 전략 계획분야 Domain I이다.
- Evaluate the regulatory environment and provide internal advice throughout the life cycle of the product (e.g., concept, development, manufacturing, marketing) to ensure compliance.
: 규정에 맞춰 규제 환경을 평가하고 제품의 수명 주기(예: 컨셉, 개발, 제조, 마케팅) 전반에 걸쳐 내부적인 조언을 제공할 수 있는가. - Perform risk/benefit analysis on product development concept for initial product viability.
: 초기 제품의 실행 가능성 평가로서 제품 개발 컨셉의 위험/이익을 분석할 수 있는가. - Determine endpoints for safety and efficacy testing at the feasibility phase to determine the ability to comply with regulatory standards.
: 규정에 맞춰 초기 feasibility 단계에서 안전성 및 유효성 평가를 위한 평가변수를 결정할 수 있는가. - Advise research and development programs to ensure regulatory compliance.
: 규정에 맞춰 연구 및 개발 (R&D) 프로그램에 조언할 수 있는가. - Provide regulatory intelligence to develop local, regional, and global regulatory strategies that include determination of regulatory classification, submission type (e.g., eCTD, electronic, paper) for regulatory applications, due diligence, and internal/external license opportunities.
: 해당 지역, 국가 및 글로벌 규제 전략을 개발하기 위해 규정 이해력을 제공할 수 있는가. 규정 분류 결정, 신청 시 제출 유형 (예: eCTD, 전자, 종이), 실사, 라이선스 in/out 기회 등을 포함함. - Evaluate the regulatory outcomes of initial product concepts and make recommendations for future actions.
: 초기 제품 컨셉에 대한 규정 결과를 평가하고 향후 조치를 제시할 수 있는가. - Evaluate and interpret regulatory decisions in a similar product category to assess regulatory implications for approval.
: 시밀러 제품의 카테고리에서 승인을 위한 규제 영향을 평가할 수 있는가. - Identify and engage appropriate regulatory authorities for submission of data concerning the product being developed.
: 개발 중인 제품을 고려하여 데이터를 제출하기 위해 적절한 규제기관을 식별하고 참여여부를 결정할 수 있는가.
- Assess impact of local, regional, and global requirements and considerations on the regulatory dossiers.
: 규정된 서류에 대해 해당 지역, 국가, 글로벌 요구사항 및 고려사항의 영향 평가를 할 수 있는가. - Consult with multidisciplinary teams to develop indications for use, intended use, and product claims (e.g., target product profile, product requirements).
: 적응증, 사용목적, 제품의도 (목표 프로파일, 제품 요구사항) 등을 개발하기 위해 여러 부서와 상의할 수 있는가. - Evaluate the regulatory merits of domestic versus regional or global submission strategies (e.g., simultaneous filings, joint reviews, mutual recognition agreements, assessment of similarity or dissimilarity of requirements) to define market feasibility.
: 시장 타당성을 정의하기 위해 해당 지역 vs 국가 또는 글로벌 제출 전략 (예: 동시 제출, 공동 검토, 상호 인정 가능여부, 요구사항의 유사성 또는 차이점)을 평가하여 규정 상 유리한 방법으로 진행할 수 있는가. - Anticipate regulatory issues arising from trade-related matters (e.g., applicable treaty law, international conventions, “for export only” status).
: 통관 관련 문제 (예: 해당 조약, 국제 협약, "수출 전용" 상태) 등으로 인해 발생할 수 있는 위험을 예상할 수 있는가. - Develop strategies for regulatory authority interactions (e.g., FDA/CA meetings, correspondence, documenting verbal communication or commitments) to guide product development life cycle management.
: 제품 개발의 수명주기 관리를 위해 규제기관 상호작용 (예: FDA/CA 미팅, 서면 의사소통, 구두 의사소통 또는 서약 문서화 등)을 고려하여 전략을 개발할 수 있는가. - Ensure regulatory compliance of company standard operating procedures impacting internal stakeholders.
: 규정에 맞도록 SOP를 평가하여 내부 이해관계자에게 미치는 영향 평가를 할 수 있는가. - Provide internal trainers with information on regulatory requirements to incorporate in ongoing training programs.
: 진행중인 교육 프로그램에 포함시킬 수 있도록 규제 요구사항들을 내부 교육자에게 지속적으로 제시할 수 있는가.
Domain I은 제품의 전반적인 개발 사이클에 따라 규정을 준수하기 위한 다양한 task에 대해 다루고 있다. 이러한 활동에는 규정 평가, 제품 컨셉 분석, 안전성 및 유효성 평가, 문제 예측과 대응 등이 포함된다.
다음 포스팅에서는 Domain II에 대해 다뤄보겠다.
'RAC 자격증' 카테고리의 다른 글
| RAPS RAC 자격증 알아보기 (1) 자격요건, 시험정보 (0) | 2024.03.01 |
|---|

댓글